 Система менеджмента качества понятие всеобъемлющее для любой деятельности, связанной с производством продукции, так как представляет собой совокупность процессов, направленных на обеспечение стабильного качества выпускаемой продукции и оказываемых услуг. Промышленность медицинских изделий так же имеет установившуюся регламентированную систему менеджмента качества (СМК), которую производитель должен внедрять, регулировать, поддерживать на своем производстве и, соответственно, сертифицировать её. Сертификат соответствия системы менеджмента качества является документальным подтверждением того, что на предприятии внедрена действующая СМК. Данный сертификат позволяет демонстрировать потребителю стабильное качество работ по проектированию, производству, сопровождению, ремонту производимой продукции.
Система менеджмента качества понятие всеобъемлющее для любой деятельности, связанной с производством продукции, так как представляет собой совокупность процессов, направленных на обеспечение стабильного качества выпускаемой продукции и оказываемых услуг. Промышленность медицинских изделий так же имеет установившуюся регламентированную систему менеджмента качества (СМК), которую производитель должен внедрять, регулировать, поддерживать на своем производстве и, соответственно, сертифицировать её. Сертификат соответствия системы менеджмента качества является документальным подтверждением того, что на предприятии внедрена действующая СМК. Данный сертификат позволяет демонстрировать потребителю стабильное качество работ по проектированию, производству, сопровождению, ремонту производимой продукции.
В настоящей статье мы:
- рассмотрим основополагающие стандарты СМК, применяемые в промышленности медицинских изделий, а также дополнительные ключевые стандарты;
- раскроем понятие СМК и обозначим факторы, оказывающие на неё влияние;
- определим необходимость предоставления сертификата соответствия системы менеджмента качества в регистрирующие органы;
- ознакомимся с примерами сертификатов соответствия системы менеджмента качества.
Основополагающими стандартами являются:
ГОСТ Р ИСО 9001-2015 (ISO 9001:2015) «Системы менеджмента качества. Требования» - общий стандарт, указывающий на основные принципы СМК. Применим к любой отрасли и сфере производства и представляет собой описание процессного подхода по планированию процессов и их взаимодействий. Структура стандарта представляет собой цикл: «Планируй-Делай-Проверяй-Действуй» (PDCA) (рисунок 1). Требования данного стандарта являются дополнительными к требованиям продукции и услугам.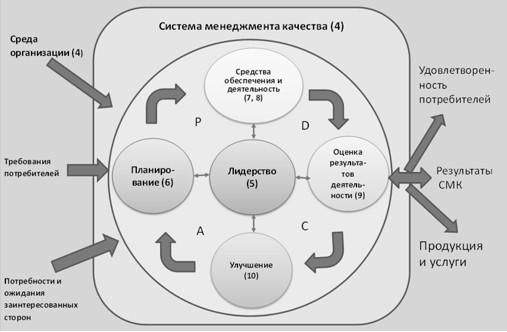
Рисунок 1 - Изображение структуры ГОСТ Р ИСО 9001-2015 в соответствии с циклом PDCA, где цифры в скобках являются ссылками на разделы стандарта
ГОСТ ISO 13485-2017 (ISO 13485:2016) «Изделия медицинские. Системы менеджмента качества. Требования для целей регулирования» - стандарт устанавливает основные требования к СМК в производстве медицинских изделий. Регламентирует требования на всех стадиях жизненного цикла медицинского изделия: проектирование и разработка (рисунок 2), производство, хранение и поставка, монтаж, техническое обслуживание, окончательный вывод из эксплуатации и утилизацию медицинских изделий или предоставление связанных с ним услуг.
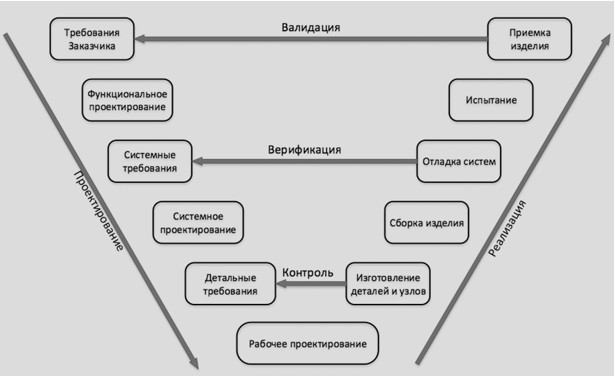
Рисунок 2 – Проектирование и разработка согласно ГОСТ ISO 13485
Дополнительные ключевые стандарты:
ГОСТ ISO 14971-2011 (ISO 14971:2007) «Изделия медицинские. Применение менеджмента риска к медицинским изделиям» - стандарт предназначен для осуществления изготовителями результативного менеджмента всех рисков, связанных с применением медицинских изделий. Документ «Файл менеджмента риска на медицинское изделие» (ФМР) указывает на проделанную работу производителем медицинских изделий при определении рисков, связанных с применением изделия, их оценки и введенных в связи с ними ограничений, а также информацию по проведению принятых мер.
ГОСТ Р МЭК 62366-2013 (IEC 62366:2007) «Изделия медицинские. Проектирование медицинских изделий с учетом эксплуатационной пригодности» - стандарт предназначен для подтверждения того, что медицинское изделие достигает разумного уровня эксплуатационной пригодности, который в свою очередь предназначен для минимизации пользовательских ошибок и минимизации рисков, связанных с использованием медицинского изделия. Документ «Файл проектирования с учетом эксплуатационной пригодности» (ФПЭП) включает в себя спецификацию эксплуатационной пригодности, основные рабочие функции, сценарии использования изделия, требования к пользовательскому интерфейсу для основных рабочих функций, анализ риска, оценку риска и приемлемость остаточных рисков.
ГОСТ Р МЭК 62304-2013 (IEC 62304:2006) «Изделия медицинские. Программное обеспечение. Процессы жизненного цикла» - стандарт применим к медицинским изделиям, имеющим в своем составе, как неотъемлемую часть, программного обеспечение. Документом, подтверждающим соответствие программного обеспечения требованиям настоящего стандарта, является «Файл жизненного цикла проектирования и разработки программного обеспечения медицинского изделия» (ФЖЦПО).
ГОСТ Р 56894-2016/GHTF/SG1/N063:2011 «Сводный комплект технической документации для демонстрации соответствия общим принципам обеспечения безопасности и основных функциональных характеристик медицинских изделий для диагностики in vitro» - стандарт предназначен для подтверждения того, что производитель медицинского изделия подготовил техническую документацию на свои изделия и поддерживает ее в рабочем состоянии, а также обеспечивает своевременный доступ к данной технической документации, демонстрирующей, как было разработано, спроектировано и изготовлено медицинское изделие.
Все документы, разрабатываемые на основе дополнительных ключевых стандартов производителем медицинских изделий, являются неотъемлемой частью подтверждения внедренной и поддерживаемой СМК.
Понятие СМК и факторы, оказывающие на неё влияние
СМК – это сеть взаимосвязанных и взаимодействующих процессов, управляемая обученными ответственными лицами в соответствии с требованиями стандарта(ов) и поддерживаемая ресурсами (человеческие ресурсы, инфраструктура, производственная среда, знания), документированными процедурами (СТО, регламенты, положения, инструкции и пр.), постоянным мониторингом и изменением результативности, внутренними аудитами и функционирующая в соответствии с политикой в области качества и установленными количественно измеряемыми целями.
- факторы, относящиеся к ее намерениям и стратегическому направлению и влияющие на ее способность достигать намеченных результатов ее СМК,
- а также факторы, которые могут привести к отклонению от запланированных результатов процессов и СМК организации, использовать предупреждающие средства управления для минимизации негативных последствий и максимального использования возникающих возможностей.
Факторы, которые влияют на разработку и внедрение СМК организации согласно ГОСТ ISO 13485, приведены на рисунке 3.

Рисунок 3 - Факторы, влияющие на разработку и внедрение СМК
Итогом разработки и внедрения СМК на производстве является получение государственного или международного сертификата соответствия системы менеджмента качества.
Сертификат соответствия системы менеджмента качества
Сертификат соответствия системы менеджмента качества выдается в том случае, если производитель медицинского изделия смог подтвердить внедренную на производстве, работающую и отвечающую всем требованиям стандартов СМК, утвержденную и одобренную в ходе проведения независимой проверки СМК третьей стороной с последующей выдачей сертификата соответствия. В качестве третьей стороны выступает орган по сертификации. Орган по сертификации выносит свое заключение в ходе проведения аудиторской проверки. Сертификат свидетельствует о том, что на производстве проведена проверка работы действующей на предприятии СМК, и результаты данной проверки признаны достаточными для выдачи сертификата соответствия менеджмента качества.
Для государственной регистрации медицинского изделия в регистрирующем органе (Росздравнадзоре) на территории Российской Федерации зачатую необходимо предоставление сертификата соответствия системы менеджмента качества.
Так, если медицинское изделие изготавливается на территории иностранного государства сертификат соответствия системы менеджмента качества должен быть предоставлен в комплекте регистрационного досье в обязательном порядке. В случае, когда предприятие имеет сразу два сертификата соответствия системы менеджмента качества ISO 9001:2015 и ISO 13485:2016 (рисунок 4) достаточно предоставление только одного из них. Предпочтительнее прикладывать в комплект регистрационного досье на медицинское изделие сертификат соответствия системы менеджмента качества ISO 13485:2016.
Для медицинских изделий отечественного производства на момент написания статьи сертификат соответствия системы менеджмента качества к предоставлению в регистрирующий орган не является обязательным. Тем не менее, с 01.01.2022 года в силу вступают единые требования для регистрации медицинских изделий в рамках Евразийского экономического союза, где сертификат соответствия системы менеджмента качества уже будет являться необходимым документом. Пример сертификата соответствия системы менеджмента качества ГОСТ ISO 13485-2017, выданного на территории Российской Федерации, приведен на рисунке 5.

Рисунок 4 – Пример Сертификата соответствия системы менеджмента качества ISO 13485:2016 на медицинское изделие иностранного производства






