 Для подтверждения технической готовности организации к изготовлению медицинских изделий в соответствии с требованиями технической документации и действующего законодательства, производитель должен предоставить информацию по проектированию и производству медицинского изделия. Для этого он должен реализовать основные стадии, этапы разработки и проектирования изделия, заканчивающиеся выпуском первой промышленной партии изделия и проведением квалификационных испытаний.
Для подтверждения технической готовности организации к изготовлению медицинских изделий в соответствии с требованиями технической документации и действующего законодательства, производитель должен предоставить информацию по проектированию и производству медицинского изделия. Для этого он должен реализовать основные стадии, этапы разработки и проектирования изделия, заканчивающиеся выпуском первой промышленной партии изделия и проведением квалификационных испытаний.
Квалификационные испытания представляют собой контрольные испытания установочной серии или первой промышленной партии, проводимые с целью оценки готовности предприятия к выпуску продукции данного типа в заданном объеме.
Обозначим основные стадии и этапы разработки и проектирования изделий:
1. Разработка эскизно-технического проекта изделия;
2. Разработка дизайна изделия;
3. Разработка рабочей конструкторской документации на изделие;
4. Разработка технологической документации на изделие;
5. Изготовление опытного образца изделия;
6. Проведение предварительных испытаний опытного образца;
7. Корректировка конструкторской документации;
8. Проведение приемочных испытаний опытных образцов;
9. Разработка технического регламента для организации серийного производства;
10. Выпуск первой промышленной партии изделия;
11. Проведение квалификационных испытаний.
После выпуска первой партии изделий приказом изготовителя формируется состав квалификационной комиссии для проведения квалификационных испытаний. Квалификационные испытания организует и обеспечивает их проведение по утвержденной программе изготовитель. Изготовитель должен проводить квалификационные испытания собственными силами и средствами. В случае, если изготовитель имеет Договор на выполнение работ по производству продукции со сторонней организацией, квалификационные испытания должны быть проведены в месте производства изделия в составе членов комиссии с каждой стороны совместно.
В состав комиссии должны входить представители разработчика, изготовителя и, при необходимости, органов государственного надзора и других заинтересованных сторон. Каждый член комиссии должен иметь соответствующую квалификацию. В качестве членов комиссии могут быть задействованы: главный инженер, инженер-технолог, технический директор, представитель ОТК и т.д. Председателем комиссии, как правило, назначается директор предприятия-производителя или иной представитель изготовителя.
Целью квалификационной комиссии является организация и проведение квалификационных испытаний образцов медицинского изделия порядком постановки медицинских изделий на производство по ГОСТ Р 15.013-2016 с учетом требований ГОСТ Р 15.301-2016.
Программа квалификационных испытаний должна быть составлена по методике, разработанной и утвержденной изготовителем и охватывать объем периодических испытаний, указанных в ТУ, а также другие испытания и проверки, позволяющие достигнуть цели квалификационных испытаний.
На квалификационную комиссию изготовитель продукции в обязательном порядке представляет следующие документы:
- утвержденную программу и методику квалификационных испытаний;
- протоколы испытаний и проверок образцов продукции из установочной серии, проведенных в рамках квалификационных испытаний, включая приемо-сдаточные, и другие отчетные документы, предусмотренные программой и методикой квалификационных испытаний;
- полный комплект технической документации, разработанный и использовавшийся для изготовления установочной серии;
- справку о поверке/калибровке средств измерений, аттестации технологического и испытательного оборудования, задействованных для изготовления продукции в соответствии с технической документацией.
По факту проведения квалификационных испытаний оформляют Протокол. В протоколе испытаний отражают фактические данные проверок, осмотров, контроля, измерений и другие данные. Положительные результаты оформляются в виде Акта квалификационных испытаний. Данный документ входит в перечень документов регистрационного досье, предназначенных для предоставления в РЗН с целью государственной регистрации медицинских изделий.
Результаты квалификационных испытаний считают положительными, если продукция (установочная серия) выдержала испытания по всем пунктам программы квалификационных испытаний, положительно оценена технологическая оснащенность производства и стабильность технологического процесса изготовления для возможности выпуска в заданных объемах продукции, соответствующей конструкторской, а также технической документации. При положительных результатах квалификационных испытаний освоение производства считается законченным.
Протокол и Акт должны быть подписаны членами комиссии и лицами, участвующими в конкретном виде испытаний. Акт должен быть утвержден председателем комиссии.
Акт квалификационных испытаний содержит следующую информацию:
- даты проведения испытаний;
- наименование медицинского изделия и его производитель;
- состав комиссии;
- количество единиц продукции, подвергаемых испытаниям и проверкам;
- состав рассмотренных в процессе работы документов;
- объем квалификационных испытаний;
- полноту выполнения программы, объективность и достоверность результатов проведенных квалификационных испытаний;
- соответствие продукции обязательным требованиям технической и конструкторской документации;
- результаты рассмотрения представленных комиссии материалов;
- оценка готовности изготовителя к производству серийной продукции для реализации;
- оценка готовности конструкторской и технической документации к утверждению в установленном порядке ТУ с присвоением литера А.
Форма акта квалификационных испытаний приведена на рисунке ниже.

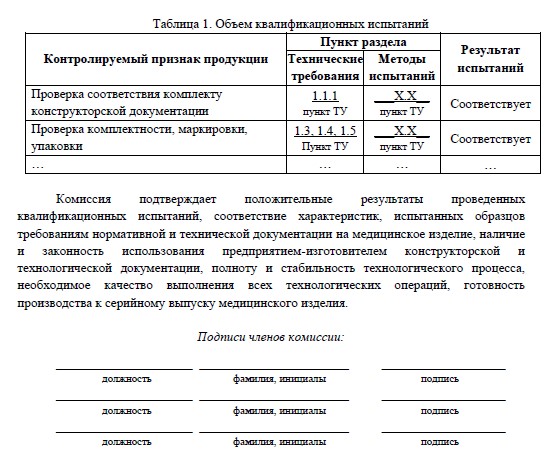
Рисунок 1 – Форма Акта квалификационных испытаний





