9 апреля 2020 года Федеральной службой по надзору в сфере здравоохранения (Росздравнадзор) было выдано регистрационное удостоверение № РЗН 2020/9918 на медицинское изделие: «Соединители для дыхательного контура» производства «Медерен Неотех Лтд. (Mederen Neotech Ltd.)», Израиль, уполномоченный представитель производителя медицинского изделия: Общество с ограниченной ответственностью "АЛЬФАМЕДЭКС"(ООО "АЛЬФАМЕДЭКС"), Россия, 197229, город Санкт-Петербург, проспект Лахтинский, дом 113, корпус ЛИТЕР А, офис 2.
Медицинское изделие: «Соединители для дыхательного контура» используется
для подключения дыхательного контура к средству для обеспечения
проходимости дыхательных путей (например, эндотрахеальная трубка) для
повышения мобильности края контура на стороне пациента.
Как элемент дыхательного контура используется у пациентов на искусственной вентиляции лёгких, при наркозе, в послеоперационном периоде, а также при острых и хронических состояниях, сопровождающихся нарушениями дыхательной функции.
Изделие применяется в анестезиологии и интенсивной терапии, врачами, фельдшерами и другим средним медицинским персоналом в условиях стационара, амбулатории, в машинах скорой медицинской помощи. Изделие стерильное для однократного применения.
Существует множество вариантов исполнения данного медицинского изделия, вот несколько примеров:
- Соединители для дыхательного контура конфигурируемые.
- Соединители для дыхательного контура конфигурируемые, порт для бронхоскопии и санации.
- Соединители для дыхательного контура гладкоствольные.
- Соединители для дыхательного контура гладкоствольные, порт для бронхоскопии и санации.
- Соединители для дыхательного контура гофрированные.
- Соединители для дыхательного контура гофрированные, порт для бронхоскопии и санации.
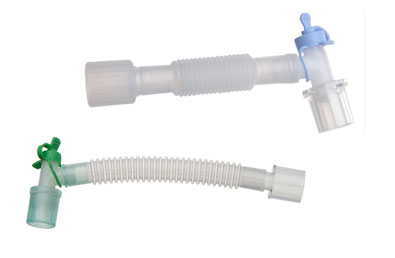
Изделие представляет собой гибкую, с коннекторами на дистальном и проксимальном концах. В зависимости от варианта исполнения, изделие может быть оснащено портом, расположенным на коннекторе дистального конца.
В зависимости от варианта исполнения изделия трубка может быть: конфигурируемой, гладкоствольной и гофрированной. Конфигурируемая трубка позволяет придать соединителю необходимую форму, а также регулировать его длину. Гладкоствольная трубка обладает низким сопротивлением потока газа и низкой турбулентностью.
В зависимости от варианта исполнения изделия коннектор, расположенный на дистальном конце может быть: прямой, угловой, двойной вертлюжный. Вертлюжный коннектор позволяет изделию совершать вращательные движения вокруг оси, уменьшая риск разъединения.
Порт, расположенный на дистальном конце изделия, в зависимости от варианта исполнения может быть: для бронхоскопии и санации, для капнографии.
Для подтверждения соответствия медицинского изделия требованиям нормативных документов Сотрудниками ООО «Невасерт» были организованы все необходимые исследования и испытания для подтверждения качества и безопасности медицинского изделия, которые проводились в соответствующих аккредитованных лабораториях, имеющих полномочия на проведение работ по исследованиям и испытаниям.
Испытательной лабораторией была проведена оценка результатов технических испытаний в форме проведения испытаний и анализа данных на медицинское изделие: «Соединители для дыхательного контура», на соответствие требованиям: ГОСТ Р 50444-92, ГОСТ 31518.1-2012, ГОСТ 31517-2012, ГОСТ Р ИСО 15223-1-2014, ГОСТ ISO 11607-1-2018, технической документации и Инструкции по эксплуатации.
Для проведения технических испытаний были представлены:
По результатам технических испытаний было сделано следующее заключение:
Центром контроля качества были проведены токсикологические исследования медицинского изделия: «Соединители для дыхательного контура», в вариантах исполнения.
Для проведения токсикологических исследований были представлены:
После оценки результатов исследований Изделия были сделаны выводы:
Федеральным государственным учреждением, имеющем полномочия на проведение работ по испытаниям, была проведена оценка результатов клинических испытаний в форме оценки и анализа клинических данных в соответствии с нормативной документацией, с эксплуатационной и технической документацией на медицинское изделие, а также утвержденной программой клинических испытаний.
Для проведения клинических испытаний были представлены:
- Заявление на проведение клинических испытаний.
- Разрешение Росздравнадзора на проведения клинических испытаний.
- Акт оценки результатов технических испытаний медицинского изделия.
- Заключение по результатам токсикологических исследований.
- Сведения о нормативной документации, требованиям которых соответствует медицинское изделие.
- Выписка из технической документации.
- Инструкция по применению.
- Фотографические изображения общего вида медицинского изделия.
- Документы (материалы), содержащие данные о клиническом применении медицинского изделия, в том числе за пределами Российской Федерации, в том числе обзоры, отчеты о проведенных научных исследованиях, публикации, доклады, анализ риска применения, методы применения медицинского изделия.
- Образцы медицинского изделия в вариантах исполнения.
В процессе проведения клинических испытаний были исследованы:
- Назначение медицинского изделия, установленное производителем.
- Представленная техническая и эксплуатационная документация.
- Функциональные качества медицинского изделия, эффективность его применения, показания и противопоказания к его применению.
- Эксплуатационные качества медицинского изделия, возможности управления и удобство обращения с ним, техническая эстетика медицинского изделия, его оформление, устойчивость к дезинфекции, стерилизации.
- Информация об обнаруженных в процессе клинических испытаний недостатках конструкции и качества медицинского изделия (при наличии), особенности работы с ним в процессе эксплуатации.
- Сведения о взаимозаменяемых медицинских изделиях.
По результатам клинических испытаний были сделаны выводы:
Для регистрации медицинского изделия «Соединители для дыхательного контура» специалистами компании «Невасерт» был разработан и подан в Росздравнадзор пакет документов:
- Заявление о регистрации медицинского изделия.
- Разрешение на ввоз медицинского изделия с целью его государственной регистрации.
- Выписка из технической документации на медицинское изделие.
- Инструкция по применению медицинского изделия.
- Паспорта безопасности материалов на медицинское изделие.
- Сведения о нормативной документации на медицинское изделие.
- Фотографические изображения общего вида медицинского изделия.
- Доверенность от фирмы-производителя на регистрацию медицинского изделия в Российской Федерации.
- Платежное поручение об уплате государственной пошлины за регистрацию медицинского изделия.
- Платежное поручение об уплате государственной пошлины за проведение экспертизы качества, эффективности и безопасности медицинского изделия.
- Документы, подтверждающие регистрацию организации-изготовителя.
- Документы, подтверждающие соответствие условий производства медицинского изделия требованиям законодательства Российской Федерации.
- Документы, подтверждающие соответствие условий производства медицинского изделия требованиям законодательства Российской Федерации.
- Акт оценки результатов технических испытаний.
- Заключение по результатам токсикологических исследований.

Рис. 1 Благодарственное письмо от ООО "АЛЬФАМЕДЭКС".
Сканер-копии документов выложены с разрешения ООО "АЛЬФАМЕДЭКС".

Рис. 2 Регистрационное удостоверение на медицинское изделие «Соединители для дыхательного контура» производства «Медерен Неотех Лтд.», Израиль,










