28 января 2020 года Федеральной службой по надзору в сфере здравоохранения (Росздравнадзор) было выдано регистрационное удостоверение № РЗН 2019/8818 на медицинское изделие: «Маски анестезиологические» производства «Медерен Неотех Лтд. (Mederen Neotech Ltd.)», Израиль, уполномоченный представитель производителя медицинского изделия: Общество с ограниченной ответственностью "АЛЬФАМЕДЭКС"(ООО "АЛЬФАМЕДЭКС"), Россия, 197229, город Санкт-Петербург, проспект Лахтинский, дом 113, корпус ЛИТЕР А, офис 2.
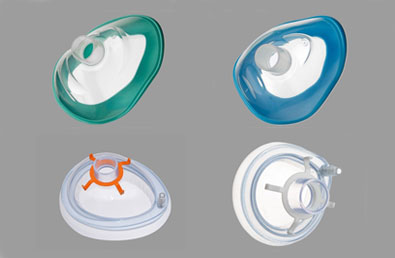
Медицинское изделие: «Маски анестезиологические» используется для проведения ингаляционного наркоза пациента и/или искусственной вентиляции лёгких.
Принцип действия: Маску удерживают на лице пациента большим и указательным пальцем. За счет специальной манжеты или ободка приспособление прилегает к лицу плотно и герметично. Посредством специального анестезиологического коннектора, можно подсоединить дыхательный контур или аппарат ручной вентиляции лёгких. Через маску осуществляется подача воздуха, кислорода и/или наркозных газовых смесей самостоятельно дышащему пациенту или в качестве вспомогательной, либо контролируемой искусственной вентиляции лёгких пациенту с недостаточным самостоятельным дыханием или при его полном отсутствии. При правильном положении маски дыхательные пути открыты, самостоятельное дыхание не затруднено, а искусственная вентиляция лёгких осуществляется легко и без сопротивления. В противном случае поправляют положение изделия, добиваясь его герметичного прилегания к лицу пациента.
Изделие предназначено для применения врачами анестезиологами-реаниматологами, а также персоналом, прошедшим необходимое обучение в условиях стационара, каретах скорой помощи. Изделие является неинвазивным устройством и предназначено для краткосрочного применения.
Маски изготавливаются следующих размеров:
- Неонатальные - для младенцев, размер: 0.
- Педиатрические - для детей, размеры: 1; 2.
- Стандартные - для взрослых, размеры: S; M; L; XL.
Маски разработаны на основании исследований строения человеческого лица, плотно и герметично прилегают гибкой, мягкой манжетой/вкладышем к лицу.
Маски делятся на два типа:
- С подкачиваемый манжетой - возможность подкачки манжеты через клапан в целях большей герметизации и прилеганию маски к конкретному, индивидуальному лицу пациента.
- С вкладышем. Вкладыш не имеет возможности подкачки, но также имеет эффективные герметизацию и прилегание к лицу пациента.
В обоих случаях пациент не испытывает дискомфорта при эксплуатации масок.
Для подтверждения соответствия медицинского изделия требованиям нормативных документов Сотрудниками ООО «Невасерт» были организованы все необходимые исследования и испытания для подтверждения качества и безопасности медицинского изделия, которые проводились в соответствующих аккредитованных лабораториях, имеющих полномочия на проведение работ по исследованиям и испытаниям.
Испытательной лабораторией была проведена оценка результатов технических испытаний в форме проведения испытаний и анализа данных на медицинское изделие: «Маски анестезиологические», на соответствие требованиям: ГОСТ Р 50444-92, ГОСТ ISO 11607-2011, ГОСТ Р ИСО 15223-1-2014, технической документации и инструкции по применению.
Для проведения технических испытаний были представлены:
- Маски анестезиологические в вариантах исполнения.
- Заявка о проведении технических испытаний.
- Инструкция по применению;
- Выписка из технической документации;
- Файл менеджмента риска;
- Заключение токсикологических исследований
- Отчет о валидации процесса стерилизации
- Фотографические изображения общего вида медицинского изделия.
По результатам технических испытаний было сделано следующее заключение:
Лабораторным центром были проведены токсикологические исследования медицинского изделия «Маски анестезиологические» (в вариантах исполнения).
Для проведения токсикологических исследований были представлены:
- Заявление о проведении исследований.
- Сведения о нормативной документации на медицинское изделие
- Техническая и эксплуатационная документация с перечнем национальных и межгосударственных стандартов, требованиям которых соответствует медицинское изделие.
- Образцы медицинского изделия в вариантах исполнения.
После оценки результатов исследований Изделия были сделаны выводы:
Медицинским исследовательским центром, имеющем полномочия на проведение работ по испытаниям, была проведена оценка результатов клинических испытаний в форме оценки и анализа клинических данных в соответствии с нормативной документацией, с эксплуатационной и технической документацией на медицинское изделие, а также утвержденной программой клинических испытаний.
Для проведения клинических испытаний были представлены:
- Заявление на проведение клинических испытаний.
- Разрешение Росздравнадзора на проведение клинических испытаний.
- Сведения о нормативной документации.
- Эксплуатационная документация производителя.
- Техническая документация производителя.
- Фотографические изображения медицинского изделия.
- Результаты технических испытаний.
- Результаты токсикологических испытаний.
- Сведения о взаимозаменяемых медицинских изделиях.
- Документы (материалы), содержащие данные о клиническом применении медицинского изделия, в том числе за пределами Российской Федерации, в том числе обзоры, отчеты о проведенных научных исследованиях, публикации, доклады, анализ риска применения, методы применения медицинского изделия:
В процессе проведения клинических испытаний были исследованы:
- Назначение медицинского изделия, установленное производителем.
- Представленная техническая и эксплуатационная документация.
- Функциональные качества медицинского изделия, эффективность его применения, показания и противопоказания к его применению.
- Эксплуатационные качества медицинского изделия, возможности управления и удобство обращения с ним, техническая эстетика медицинского изделия, его оформление, устойчивость к дезинфекции, стерилизации.
- Информация об обнаруженных в процессе клинических испытаний недостатках конструкции и качества медицинского изделия (при наличии), особенности работы с ним в процессе эксплуатации.
- Сведения о взаимозаменяемых медицинских изделиях.
По результатам клинических испытаний были сделаны выводы:
Для регистрации медицинского изделия «Маски анестезиологические» специалистами компании «Невасерт» был разработан и подан в Росздравнадзор пакет документов:
- Заявление о регистрации медицинского изделия.
- Разрешение на ввоз медицинского изделия с целью его государственной регистрации.
- Выписка из технической документации на медицинское изделие.
- Инструкция по применению медицинского изделия.
- Паспорта безопасности материалов на медицинское изделие.
- Сведения о нормативной документации на медицинское изделие.
- Фотографические изображения общего вида медицинского изделия.
- Доверенность от фирмы-производителя на регистрацию медицинского изделия в Российской Федерации.
- Платежное поручение об уплате государственной пошлины за регистрацию медицинского изделия.
- Платежное поручение об уплате государственной пошлины за проведение экспертизы качества, эффективности и безопасности медицинского изделия.
- Документы, подтверждающие регистрацию организации-изготовителя.
- Документы, подтверждающие соответствие условий производства медицинского изделия требованиям законодательства Российской Федерации.
- Документы, подтверждающие соответствие условий производства медицинского изделия требованиям законодательства Российской Федерации.
- Акт оценки результатов технических испытаний.
- Заключение по результатам токсикологических исследований.

Рис. 1 Благодарственное письмо от ООО "АЛЬФАМЕДЭКС.
Сканер-копии документов выложены с разрешения ООО "АЛЬФАМЕДЭКС.

Рис.2 Регистрационное удостоверение на медицинское изделие «Маски анестезиологические» производства «Медерен Неотех Лтд. (Mederen Neotech Ltd.)», Израиль
Рис.3 Приложения к Регистрационному удостоверению на медицинское изделие «Маски
анестезиологические» производства «Медерен Неотех Лтд. (Mederen Neotech
Ltd.)», Израиль







