11 июня 2020 года Федеральной службой по надзору в сфере здравоохранения (Росздравнадзор) было выдано регистрационное удостоверение № РЗН 2020/10713 на медицинское изделие: «Катетер пупочный» производства «Медерен Неотех Лтд. (Mederen Neotech Ltd.)», Израиль, уполномоченный представитель производителя медицинского изделия: Общество с ограниченной ответственностью "АЛЬФАМЕДЭКС"(ООО "АЛЬФАМЕДЭКС"), Россия, 197229, город Санкт-Петербург, проспект Лахтинский, дом 113, корпус ЛИТЕР А, офис 2.
Медицинское изделие «Катетер пупочный» (далее – Изделие, Катетер) применяется в медицинских учреждениях, врачом-специалистом для катетеризации пупочной вены новорожденных с целью обеспечения эффективного венозного доступа.
Изделие – стерильное и предназначено для однократного применения одним пациентом.
Катетер пупочный выпускается в трех различных размерах.
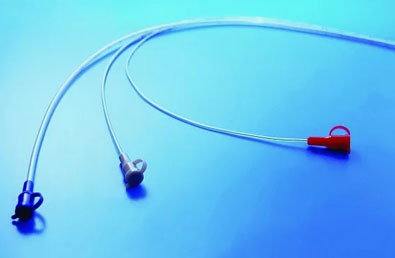
Изделие состоит из трубки и коннектора с цветовой кодировкой, которая позволяет определить размер изделия. Дистальный конец изделия открыт и закруглен для обеспечения безопасной установки. Изделие не имеет боковых отверстий, устойчиво к перегибанию и перекручиванию.
Изделие снабжено по всей длине рентгеноконтрастной линией для проверки установки катетера. Рентгеноконтрастная линия представляет собой композиционный материал, состоящий из связующего полимера (поливинилхлорид) и наполнителя (бария сульфат), который хорошо поглощает рентгеновское излучение. Для лучшей визуализации рентгеноконтрастной линии используется синий краситель.
Изделие имеет Луер-коннектор, оснащенный герметично закрывающейся пробкой препятствующей вытеканию жидкости и заражению содержимого изделия.
Для подтверждения соответствия медицинского изделия требованиям нормативных документов Сотрудниками ООО «Невасерт» были организованы все необходимые исследования и испытания для подтверждения качества и безопасности медицинского изделия, которые проводились в соответствующих аккредитованных лабораториях, имеющих полномочия на проведение работ по исследованиям и испытаниям.
Испытательной лабораторией была проведена оценка результатов технических испытаний в форме проведения испытаний и анализа данных на медицинское изделие: «Катетер пупочный, в вариантах исполнения», на соответствие требованиям ГОСТ Р 50444-92, ГОСТ ISO 11607-1-2018, ГОСТ Р ИСО 15223-1-2014, Выписки из технической документации и Инструкции по применению.
Для проведения технических испытаний были представлены:
- Образец медицинского изделия (Катетер пупочный).
- Заявка от о проведении технических испытаний медицинского изделия.
- Инструкция по применению.
- Выписка из технической документации.
- Заключение по результатам токсикологических исследований.
- Файл менеджмента риска.
- Фотографические изображения общего вида медицинского изделия.
По результатам технических испытаний было сделано следующее заключение:
Лабораторным центром были проведены токсикологические исследования медицинского изделия «Катетер пупочный» производства Медерен Неотех Лтд., Израиль.
Для проведения токсикологических исследований были представлены:
- Заявление о проведении исследований.
- Сведения о нормативной документации на медицинское изделие
- Техническая и эксплуатационная документация с перечнем национальных стандартов, требованиям которых соответствуют медицинское изделие.
- Образцы медицинского изделия, в вариантах исполнения.
После оценки результатов исследований Изделия были сделаны выводы:
Исследовательским центром была проведена оценка результатов клинических испытаний в форме оценки и анализа клинических данных.
Для проведения клинических испытаний были представлены:
- Заявление на проведение клинических испытаний.
- Разрешение на проведение клинических испытаний.
- Акт оценки результатов технических испытаний медицинского изделия.
- Заключение по результатам токсикологических исследований.
- Сведения о нормативной документации на медицинское изделие, требованиям которой соответствует медицинское изделие.
- Выписка из технической документации.
- Руководство по эксплуатации.
- Фотографические изображения общего вида медицинского изделия.
- Документы (материалы), содержащие данные о клиническом применении медицинского изделия, в том числе за пределами Российской Федерации, в том числе обзоры, отчеты о проведенных научных исследованиях, публикации, доклады, анализ риска применения, методы применения медицинского изделия.
- Сведения о взаимозаменяемом медицинском изделии.
- Образец медицинского изделия.
Вот некоторые из этапов проведения клинических испытаний:
- Анализ технической и эксплуатационной документации.
- Изучение функциональных качеств медицинского изделия, эффективности его применения, показаний и противопоказаний к его применению.
- Исследование эксплуатационных качеств медицинского изделия, возможностей управления и удобства обращения с ним, технической эстетики медицинского изделия, его оформления, устойчивости к дезинфекции, стерилизации.
- Изучение информации об обнаруженных в процессе клинических испытаний недостатках конструкции и качества медицинского изделия (при наличии), особенности работы с ним в процессе эксплуатации.
- Определение потенциального риска медицинского изделия.
- Анализ риска применения.
По результатам клинических испытаний были сделаны выводы:
Для регистрации медицинского изделия «Катетер пупочный» специалистами компании «Невасерт» был разработан и подан в Росздравнадзор пакет документов:
- Заявление о государственной регистрации медицинского изделия с описью документов.
- Техническая документация производителя на медицинское изделие.
- Инструкция по применению медицинского изделия.
- Сведения о нормативной документации на медицинское изделие.
- Фотографические изображения общего вида медицинского изделия.
- Доверенность от фирмы-производителя на регистрацию медицинского изделия в Российской Федерации.
- Копия разрешения на ввоз.
- Платежное поручение об уплате государственной пошлины за регистрацию медицинского изделия.
- Платежное поручение об уплате государственной пошлины за проведение экспертизы качества, эффективности и безопасности медицинского изделия.
- Документы, подтверждающие регистрацию организации-изготовителя.
- Документы, подтверждающие соответствие условий производства медицинского изделия требованиям законодательства Российской Федерации.

Рис. 1 : Благодарственное письмо от ООО "АЛЬФАМЕДЭКС.
Сканер-копии документов выложены с разрешения ООО "АЛЬФАМЕДЭКС.

Рис. 2 : Регистрационное удостоверение на медицинское изделие «Катетер пупочный» производства «Медерен Неотех Лтд. », Израиль.

Рис. 3 : Приложение к Регистрационному удостоверению на медицинское изделие «Катетер пупочный» производства «Медерен Неотех Лтд. », Израиль.





