15 октября 2025 года Федеральной службой по надзору в сфере здравоохранения (Росздравнадзор) была произведена регистрация медицинского изделия: «Головодержатель мягкой фиксации», внесённого в Государственный реестр медицинских изделий под номером РЗН 2025/26298 (ЕРУЛ - Г004-00110- 00/04138884), производства Общества с ограниченной ответственностью «ОРТО», Россия, 190020, г. Санкт- Петербург, ул. Лифляндская, д. 6, литер М.
Медицинское изделие «Головодержатель мягкой фиксации» предназначено для мягкой степени фиксации шейного отдела позвоночника.
Потенциальные потребители: пациенты, нуждающиеся в данном медицинском изделии по показаниям или назначению врача.
Используется при следующих показаниях:
- заболевания (дорсопатии) и травмы области шеи с болями умеренной интенсивности (цервикалгия) с/без ограничения движений в шейном отделе позвоночника, в том числе:
- ушибы мягких тканей,
- растяжения и перенапряжение капсульно-связочного аппарата,
- остеохондроз и другие дегенеративные заболевания шейного отдела позвоночника,
- миофасциальный болевой синдром («шейный миозит»),
- шейный синдром (головные боли, головокружения, нарушения сна, ухудшение памяти и т.д.);
- различные периоды реабилитации после травм и операций в области шеи, шейного отдела позвоночника и черепно-мозговой травмы.
- профилактика травм и заболеваний шейного отдела позвоночника при динамических и статических нагрузках, остеопорозе, быстрой утомляемости.
Головодержатель выпускается в следующих видах:
- для недоношенных и новорожденных детей (первые 4 недели после рождения) - изделия с длиной гильзы 28 см;
- для детей грудного возраста (от 4 недель до 1 года) - изделия с длиной гильзы 32 и 33 см;
- для детей от 1 года до 7 лет - изделия с длиной гильзы 36 см;
- для детей от 7 до 15 лет - изделия с длиной гильзы 42 см;
- для взрослых - изделия с длиной гильзы 53 см.
Сфера применения: для использования в домашних условиях и в условиях лечебно-профилактических учреждений.
Для подтверждения соответствия медицинского изделия требованиям нормативных документов Сотрудниками ООО «Невасерт» были организованы все необходимые исследования и испытания для подтверждения качества и безопасности медицинского изделия, которые проводились в соответствующих аккредитованных лабораториях, имеющих полномочия на проведение работ по исследованиям и испытаниям.
Испытательным центром была проведена оценка результатов технических испытаний в форме проведения испытаний в соответствии с утверждённой программой технических испытаний на медицинское изделие: «Головодержатель мягкой фиксации» производства Общества с ограниченной ответственностью «ОРТО», Россия, в соответствии с Технической и эксплуатационной документацией на соответствие требованиям: ТУ 32.50.22-001-50910339-2024, ГОСТР 50444-2020, ГОСТ Р 59445-2021, ГОСТ Р ИСО 22523-2007, ГОСТ Р ИСО 15223-1-2023.
Для проведения технических испытаний были представлены:
- Заявка от ООО «ОРТО» на проведение испытаний.
- Образцы медицинского изделия в вариантах исполнения.
- Технические условия.
- Эксплуатационная документация.
- Файл менеджмента риска.
- Отчет об исследованиях стабильности, обосновывающий срок хранения.
- Сведения о нормативной документации.
- Фотографические изображения общего вида медицинского изделия.
По результатам технических испытаний было сделано следующее заключение:
Испытательным аналитическим центром были проведены токсикологические исследования медицинского изделия: «Головодержатель мягкой фиксации», производства ООО «ОРТО», в соответствии с утвержденной программой.
Для проведения токсикологических испытаний представлены:
- Заявка о проведении токсикологических исследований.
- Сведения о нормативной документации на медицинское изделие.
- Технические условия.
- Образцы медицинского изделия в вариантах исполнения.
По результатам проведенных испытаний были сделаны выводы:
Федеральным государственным учреждением была проведена оценка результатов клинических испытаний в форме оценки и анализа клинических данных медицинского изделия: «Головодержатель мягкой фиксации» производства Общества с ограниченной ответственностью «ОРТО», Россия, в соответствии с нормативной документацией, с технической и эксплуатационной документацией производителя, а также утвержденной программой клинических испытаний.
Для проведения клинических испытаний были представлены:
- Заявление на проведение клинических испытаний медицинского изделия.
- Фотографические изображения медицинского изделия.
- Сведения о нормативной документации.
- Эксплуатационная документация производителя.
- Техническая документация.
- Результаты технических испытаний.
- Проект программы и методики клинических испытаний.
- Образец медицинского изделия в вариантах исполнения.
- Сведения о взаимозаменяемом медицинском изделии.
- Результаты токсикологических исследований.
- Файл менеджмента риска.
- Документы (материалы), содержащие данные о клиническом применении медицинского изделия, в том числе за пределами Российской Федерации, в том числе обзоры, отчеты о проведенных научных исследованиях, публикации, доклады, анализ риска применения, методы применения медицинского изделия.
Вот некоторые этапы проведения клинических испытаний:
- Оценка предоставленной документации.
- Исследование функциональных качеств медицинского изделия, эффективности его применения, показаний и противопоказаний к его применению.
- Изучение возможностей медицинского изделия, касающихся точности измерений, достоверности, воспроизводимости, надежности.
- Исследование эксплуатационных качеств медицинского изделия, возможности управления и удобства обращения с ним, технической эстетики медицинского изделия, его оформления, устойчивости к дезинфекции, стерилизации.
- Изучение информации об обнаруженных в процессе клинических испытаний недостатках конструкции и качества медицинского изделия (при наличии), особенности работы с ним в процессе эксплуатации.
- Изучение сведений о взаимозаменяемых медицинских изделиях.
По результатам клинических испытаний были сделаны выводы:
Для регистрации медицинского изделия «Головодержатель мягкой фиксации» специалистами компании «Невасерт» был разработан и подан в Росздравнадзор пакет документов:
- Заявление о регистрации медицинского изделия.
- Технические условия ТУ 32.50.22-001-50910339-2024.
- Инструкция по применению.
- Файл менеджмента риска на медицинское изделие.
- Сведения о нормативной документации.
- Фотографические изображения медицинского изделия.
- Акт квалификационных испытаний.
- Отчет об исследованиях стабильности, обосновывающий срок хранения.
- Заключение по результатам токсикологических исследований.
- Акт оценки результатов технических испытаний медицинского изделия
- Договор аренды.
- Выписка из Единого государственного реестра юридических лиц (ЕГРЮЛ).
- Платёжные поручения.

Рис. 1 Благодарственное письмо от ООО "ОРТО"
Сканер-копии документов выложены с разрешения ООО «ОРТО».
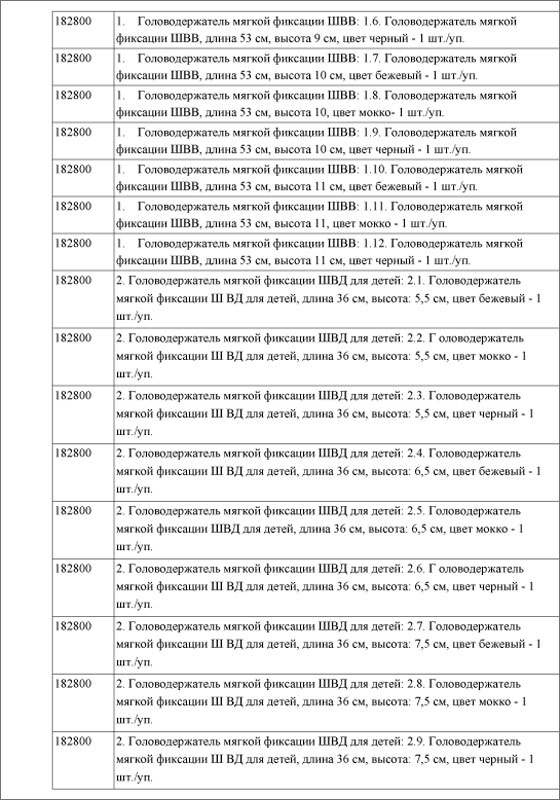
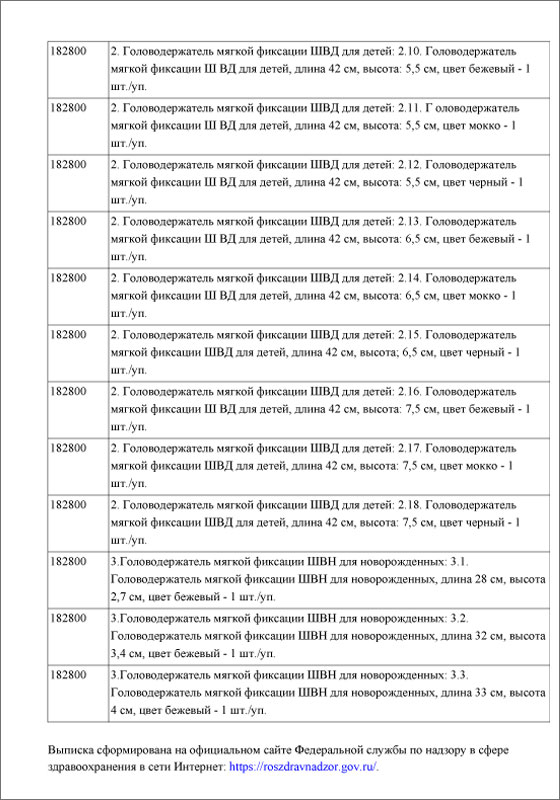
Рис. 2 Выписка из Государственного реестра медицинских изделий: «Головодержатель мягкой фиксации» производства Общества с ограниченной ответственностью «ОРТО», Россия