Медицинское изделие «ЭКГ электрод одноразовый, в вариантах исполнения» (далее Электрод, Изделие) предназначено для отведения биоэлектрических сигналов от тела пациента при длительном и кратковременном мониторинге не более 48 часов.
Электроды предназначены для использования врачом-специалистом в медицинских учреждениях с целью использования при ЭКГ-мониторинге.
Характеристика и описание Изделия:
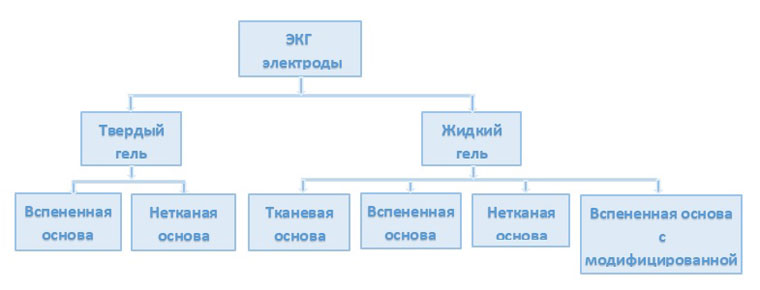
Вспененная основа - предназначена для краткосрочного мониторирования (не более 24 часов), благодаря своим водонепроницаемым свойствам позволяет использовать её у пациентов с гипергидрозом, обеспечивая надёжное сцепление с кожей, что особенно важно при проведении стресс-систем.
Нетканая основа снабжена перфорированными отверстиями, которые обеспечивают активное дыхание кожи, позволяя применять её при длительном мониторировании, в том числе у пациентов с повышенным потоотделением или при гиперчувствительности на длительный контакт с материалами различного генеза с ограничением дыхания кожных покровов (более 24 часов).
Тканевая основа по типу мягкой пергаментной материи с мелкими отверстиями для дыхания кожи позволяет не только обеспечить активное дыхание кожи, но и предотвратить нежелательное раздражения кожи во время проведения мониторинга, позволяя применять её при длительном мониторировании (более 24 часов).
Вспененная основа с модифицированной акриловой смолой с высокой адгезией, которая более устойчива к поту, и используется для стресс-теста, холтеровского мониторирования. Предназначена для краткосрочного мониторирования (не более 24 часов).
В зависимости от формы, электроды могут быть:
- круглыми;
- прямоугольными;
- каплевидным.
В зависимости от размера, электроды предназначены для следующих возрастных групп пациентов:
- для взрослых, весом более 15 кг;
- для детей, весом от 5 до 15 кг.
Одним из этапов подготовки Изделия к государственной регистрации является проведение клинических испытаний, которые должны подтвердить качество и безопасность медицинского изделия и возможность для широкого применения в клинической практике на территории Российской Федерации.
Специалистами компании «Невасерт» было организовано проведение клинических испытаний медицинского изделия «ЭКГ электрод одноразовый, в вариантах исполнения» в медицинском учреждении, полномочия которого на проведение работ по испытаниям подтверждены соответствующей лицензией.
Для проведения клинических испытаний Изделия в соответствии с нормативной, технической и эксплуатационной документацией производителя, а также утвержденной программой клинических испытаний были представлены:
- Заявление на проведение клинических испытаний.
- Сведения о нормативной документации.
- Фотографические изображения медицинского изделия.
- Эксплуатационная документация.
- Проект программы и методики клинических испытаний.
- Техническая документация медицинского изделия.
- Результаты технических испытаний.
- Образцы медицинского изделия в вариантах исполнения.
- Сведения о взаимозаменяемом медицинском изделии.
- Результаты токсикологических исследований.
- Документы (материалы), содержащие данные о клиническом применении медицинского изделия, в том числе за пределами Российской Федерации, в том числе обзоры, отчеты о проведенных научных исследованиях, публикации, доклады, анализ риска применения, методы применения медицинского изделия.
При проведении данных клинических испытаний в форме исследований (анализа и оценки клинических данных) клинические испытания медицинского изделия с участием человека не предусмотрены, в связи с чем, характеристика пациентов (количество, пол, возраст, диагноз), их информированное согласие в данном акте оценки результатов клинических испытаний отсутствуют.
Приведем примеры из перечня исследований, включенных в программу клинических испытаний:
- Анализ и оценка технической и эксплуатационной документации.
- Определение назначения медицинского изделия, среды, в которой применяется медицинское изделие, условия и правила применения, отличия медицинского изделия от аналогов.
- Определение потенциального риска Изделия.
- Изучение функциональных качеств медицинского изделия, эффективности его применения, показаний и противопоказаний к его применению.
- Исследование эксплуатационных качеств медицинского изделия, возможностей управления и удобства обращения с ним, технической эстетики медицинского изделия, его оформления, устойчивости к дезинфекции, стерилизации.
- Изучение информации об обнаруженных в процессе клинических испытаний недостатках конструкции и качества медицинского изделия (при наличии), особенности работы с ним в процессе эксплуатации.
- Анализ сведений о взаимозаменяемых медицинских изделиях.
По результатам проведенных испытаний были сделаны следующие выводы:
- Изделие соответствует требованиям нормативной документации, технической и эксплуатационной документации производителя.
- По своим эксплуатационным качествам Изделие соответствует своему медицинскому назначению и заявленным техническим характеристикам.
- Установлено удобство, надёжность и эффективность при использовании медицинского изделия.
- Медицинское изделие удобно и безопасно в ходе применения, выполнено из качественных и безопасных материалов.
- Эксплуатационная документация достаточно информативна и содержит необходимые сведения для правильного и безопасного использования медицинского изделия по назначению, его транспортирования, хранения и утилизации.
- Техническая документация содержит все необходимые сведения, регламентирующие конструкцию медицинского изделия, технические требования и характеристики, а также методы их проверки.
- Результаты клинических испытаний опытных образцов могут быть распространены на все заявленные исполнения медицинского изделия.
- Проведенный анализ показал, что медицинское изделие не уступает по качеству, эффективности и безопасности зарегистрированным аналогам и обладает теми же функциональными и эксплуатационными характеристиками, а также соответствует требованиям обязательных государственных стандартов, действующих на территории России.





