 Одним из самых волнующих заказчика вопросов, при обращении в ООО «Невасерт» является срок проведения регистрации медицинского изделия. Фирма ООО «Невасерт» одна из немногих, на данном рынке осуществляет регистрацию медицинских изделий полным циклом, иначе можно применить шаблонный запрос в поисковиках: «Регистрация медицинских изделий «под ключ».
Одним из самых волнующих заказчика вопросов, при обращении в ООО «Невасерт» является срок проведения регистрации медицинского изделия. Фирма ООО «Невасерт» одна из немногих, на данном рынке осуществляет регистрацию медицинских изделий полным циклом, иначе можно применить шаблонный запрос в поисковиках: «Регистрация медицинских изделий «под ключ». 
Чем же отличается работа по регистрации медицинских изделий с ООО «Невасерт» от других многочисленных компаний, присутствующих на этом рынке?
Профессиональная этика не позволяет нам раскрывать недобросовестные методы, которыми пользуются конкуренты. Поэтому мы лишь расскажем, как работаем сами. И только заказчику решать, с кем стоит иметь дело.
Итак, ООО «Невасерт» имеет более чем 10-ти летний опыт по регистрации медицинских изделий, так же наша компания оказала содействии в регистрации около 100 медицинских изделий. Вам покажется данное количество слишком малым, за столь большой срок, ведь другие консалтинговые фирмы хвастаются сотнями зарегистрированных в Росздравнадзоре дел.
На примере регистрационного досье компании ООО «Орторент» поясним среднестатистические сроки проведения регистрации медицинского изделия.
Во-первых, обозначим, что ООО «Невасерт» ведет усиленную работу с ООО «Орторент» на протяжении пяти лет. И у нас не возникает вопросов к ООО «Орторент» по юридической составляющей регистрационного досье. Таких, как например несоответствия заявленного места производства, договорам аренды и т.д. Кажется, подобные вопросы довольно просто решаются, однако они могут задержать процесс регистрации медицинского изделия примерно на 2-3 недели.
В июле 2016 года был заключен договор с ООО «Орторент» об оказании услуг, связанных с государственной регистрацией медицинского изделия: Подъемник для подъема и перемещения пациента. В начале декабря регистрационное досье было представлено в Росздравнадзор.
Что же было сделано за эти неполные полгода? Был разработан весь пакет технической и эксплуатационной документации (от 2-х до 3-х месяцев), так же были проведены токсикологические испытания (около 1-го месяца), после чего были проведены технические испытания (около 2-х месяцев). Технические испытания заняли довольно продолжительный срок, по причине обширности состава медицинского изделия, а также необходимости монтажных работ для работы медицинского изделия.
Далее, по тексту следуют «сухие» цифры по процедуре регистрации в Росздравнадзоре. Все сроки соблюдены в рамках законодательства Российской Федерации.
12 декабря Регистрационное досье было принято Росздравнадзором.
21 декабря регистрационное досье направлено в экспертное учреждение на экспертизу.
Уже 20-го декабря был направлен запрос о предоставлении дополнительных материалов и сведений. Для выполнения выставленных требований были необходимы корректировки Технической и Эксплуатационной документации. А также дополнительные технические испытания.
4-го апреля дополнительные материалы для регистрации медицинского изделия были приняты Росздравнадзором, а именно:
- Сопроводительное письмо (акт устранения замечаний);
- Заявление о регистрации медицинского изделия (с учетом изменений);
- Извещение №1 об изменении ТУ 9451-013-57972160-2016;
- ТУ 9451-013-57972160-2016. Технические условия (с учетом изменений);
- ОРТО.942819.002 РЭ. Руководство по эксплуатации (с учетом изменений);
- СКТД ОРТО.942819.002. Сводный комплект технической документации (с учетом изменений);
- ФМР ОРТО.942819.002-01. Файл менеджмента риска (с учетом изменений);
- ФПЭП ОРТО.942819.002-02. Файл проектирования с учетом эксплуатационной пригодности (с учетом изменений);
- Сведения о нормативной документации на медицинское изделие «Система для подъема и перемещения пациентов рельсовая медицинская «ОРТОРЕНТ ПРМ-01»;
- Фотографические изображения общего вида «Система для подъема и перемещения пациентов рельсовая медицинская «ОРТОРЕНТ ПРМ-01»;
- Дополнение к Акту оценки результатов технических испытаний.
После чего, экспертная организация обработала все дополнительные материалы и выдала 4-го мая 2017 года разрешение на проведение клинических испытаний медицинского изделия.
К 16-му июня ООО «Невасерт» подобрало аккредитованную в РЗН клинику и осуществило полное сопровождение испытаний.
Уже 11 августа экспертная организация провела проверку предоставленных документов и выставила замечания для корректировки Акта клинических испытаний.
После внесения и согласования всех необходимых корректировок. Дополнения по клиническим испытаниям были предоставлены в Росздравнадзор.
Таким образом 6 октября 2017 года на имя Общества с Ограниченной Ответсвенностью «Орторент» было выдано регистрационное удостоверение РЗН 2017/6336.
Обратим ваше внимание, что исправление замечаний РЗН на 1-м и втором этапе никак не отразилось на общих затратах заказчика.
Безусловно, в описанной статье представлен «крайний» случай, наиболее сложной и относительно долгой работы. Ниже представлена таблица сроков и этапов проведения регистрационного дела в Росздравнадзоре.
1. Дата принятия заявления | 12.12.2016 |
2. Назначение ответственного исполнителя | 13.12.2016 |
3. Проверка полноты и достоверности | Нарушений нет |
4. Принятие решения о начале регистрации | 16.12.2016 |
5. Направление задания на экспертизу (1 этап) | 21.12.2016 Направлено в экспертное учреждение задание на экспертизу |
6. Запрос материалов и сведений | 20.01.2017 Направлен запрос о предоставлении дополнительных материалов и сведений № 10-2766/17 от 20.01.2017 |
7. Ожидание дополнительных материалов | 04.04.2017 Получены дополнительные материалы |
8. Перенаправление ответа в экспертное учреждение | 13.04.2017 Дополнительные сведения от заявителя перенаправлены в экспертное учреждение |
9. Заключение о возможности направления на клинические испытания | Положительное заключение |
10. Направление на клинические испытания. Приостановление регистрации | 04.05.2017 Заявителю направлено уведомление № 10-22725/17 от 03.05.2017 о разрешении проведения клинических испытаний медицинского изделия. Регистрация приостановлена |
11. Возобновление регистрации | 15.06.2017 |
12. Направление задания на экспертизу (2 этап) | 16.06.2017 Направлено в экспертное учреждение задание на экспертизу |
13. Запрос материалов и сведений | 11.08.2017 Направлен запрос о предоставлении дополнительных материалов и сведений № 10-39494/17 от 11.08.2017 |
14. Ожидание дополнительных материалов | 13.09.2017 Получены дополнительные материалы |
15. Перенаправление ответа в экспертное учреждение | 19.09.2017 Дополнительные сведения от заявителя перенаправлены в экспертное учреждение |
16. Заключение по итогам экспертизы (2 этап) | Качество и/или эффективность и/или безопасность регистрируемого медицинского изделия подтверждены |
17. Результат | Выдано Регистрационное удостоверение № РЗН 2017/6336 от 06.10.2017. Приказ от 06.10.2017 № 8543 |
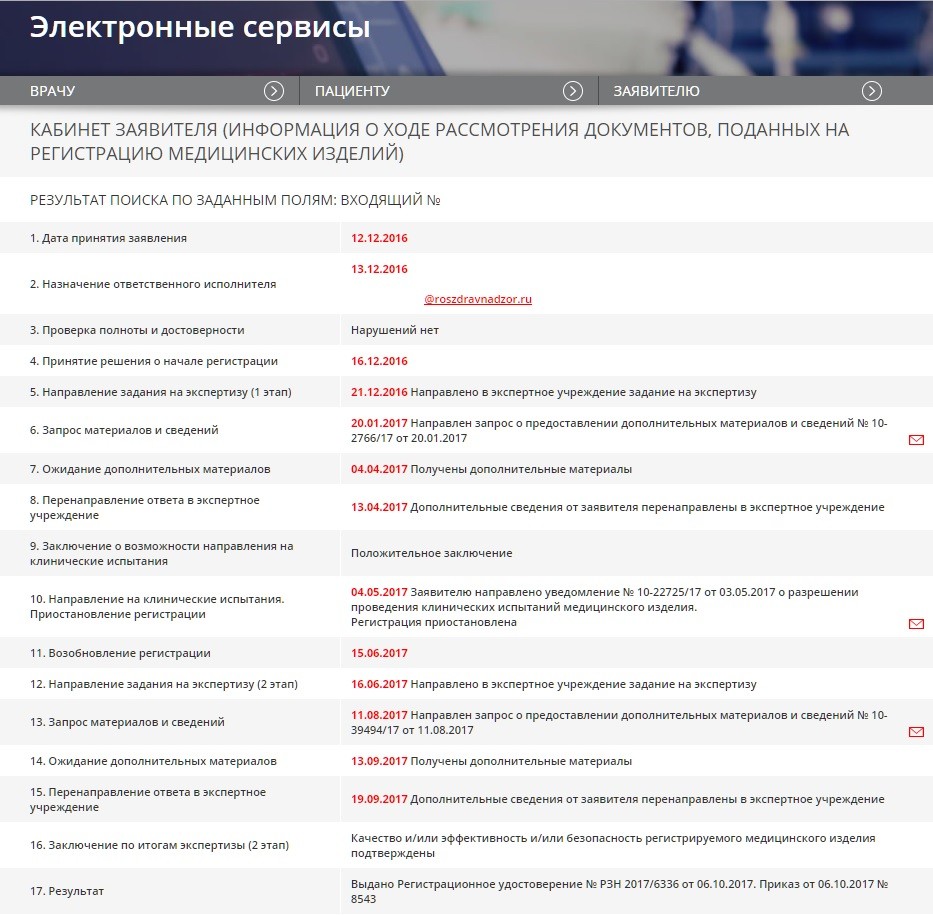
Рис. 1 - Скриншот с сайта Росздравнадзора. Кабинет заявителя. Система для подъема и перемещения пациентов рельсовая медицинская «ОРТОРЕНТ ПРМ-01»





